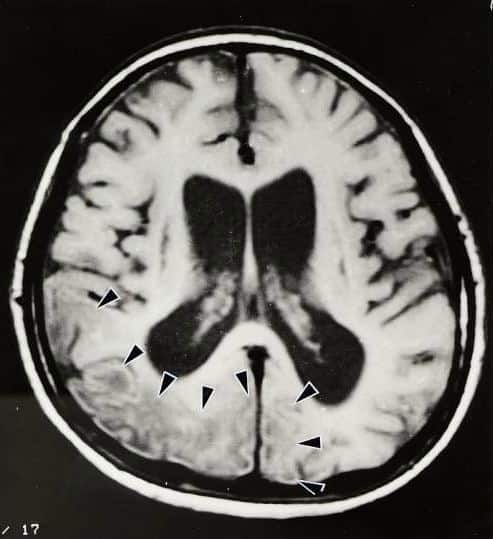
 | 後頭部(写真の左下の方で、矢尻印で囲んである部位)は薄くみえる(シグナル強度が低い)。この部は血流が少なく脳梗塞の後の所見に似る。メラスではこのように、後頭葉に病変が強い傾向がある。 病気が進行すると、本症のように脳室の拡大、脳の萎縮が目立つようになる。 |
| 図32:メラスの脳MRI(T1強調画像) | |
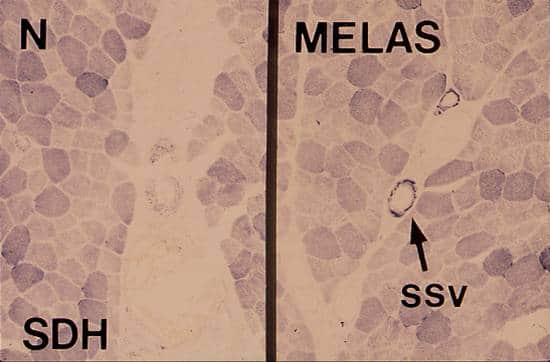 | ミトコンドリアをよく染めるコハク酸脱水素酵素(succinate dehydrogenase: SDH) 染色すると、正常筋(左:N)では血管はほとんど染まらない。 メラス(右:MELAS)では血管壁が強く染まり、異常なミトコンドリアが血管壁に蓄積していることが分かる。 |
| 図33:筋組織内の異常血管(SSV) | |
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2024/10/26 02:03 UTC 版)
ミトコンドリア脳筋症・乳酸アシドーシス・脳卒中様発作症候群 (Mitochondrial myopathy, Encephalopathy, Lactic Acidosis, Stroke-like episodes)あるいは略してMELAS(メラス)は反復する脳卒中様発作を特徴とするミトコンドリア病の一種である(以下"MELAS"と呼ぶ)。MELASの80%がmtDNAの点突然変異(3243A→G変異)により引き起こされる。

MELASはミトコンドリアの障害でATP産生がうまくいかなくなるミトコンドリア病(ミトコンドリア脳筋症)の1種である。5~15歳で好発し、知能低下や感音性難聴、低身長、易疲労性、心筋症、筋力低下といったミトコンドリア病に共通する神経・筋症状のほかに、繰り返す脳卒中様発作(頭痛・嘔吐・痙攣・意識障害・片麻痺など)が特徴的で、この発作時にCTやMRI(拡散強調画像)をとると脳梗塞に類似した病変を認める(ただし、この病変の発症機序は不明)。

ミトコンドリア病全般に共通することだが、ミトコンドリアでのATP産生(電子伝達系など)がうまくいかないことで解糖系が亢進し、血中・髄液中の乳酸濃度と乳酸/ピルビン酸比(L/P比)が上昇する。また、筋生検を行い、ゴモリ・トリクローム染色を行うと赤色ぼろ線維を認める。MELASに特徴的な所見としては、後頭部の脳梗塞類似病変や脳波での焦点周期性てんかん型放電がある。
MELASの80%はミトコンドリアDNAの点変異(3243A→G)であり、母系遺伝する。
現在、発症後の治療法は対症療法にとどまるが、2015年2月24日、英国議会上院が、ミトコンドリアDNAに異常のある女性の受精卵から核を取り出し、正常なミトコンドリアDNAを持つ女性の脱核した卵子に移植するという手法で、3人の遺伝子をもつ受精卵を誕生させ、MELASの子供への遺伝を防止する技術を承認した[1]。この治療法は、ミトコンドリア脳筋症の根治的治療法として期待される一方で、英国上院での審議では「デザイナーベビー」につながるとの倫理上の懸念から反対意見や慎重論が根強かった[1]。
2013年に日本においてもコエンザイムQ10類似の薬剤の臨床試験が開始された[2]。
川崎医科大学などの共同試験によって、アミノ酸の一種であるタウリンを大量に投与すれば発作を抑えられることがわかり、2019年1月、厚生労働省の部会でタウリンの薬の承認申請が了承された。
出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2022/06/06 04:19 UTC 版)
家族歴を有する若年性糖尿病、難聴などを特徴とするミトコンドリア脳筋症のひとつにMELAS(メラス)がある。MELASは血管壁ミトコンドリアの機能不全による痙攣発作、不全片麻痺や半盲などの脳卒中様発作を繰り返す。脳卒中様発作は後頭葉、頭頂葉でしばしば認められ、病変分布が支配領域に一致しないため脳卒中様発作と言われる。
※この「MELAS」の解説は、「脳梗塞」の解説の一部です。
「MELAS」を含む「脳梗塞」の記事については、「脳梗塞」の概要を参照ください。
固有名詞の分類