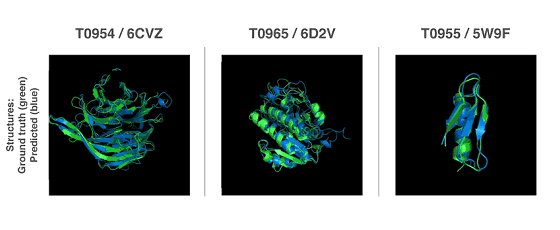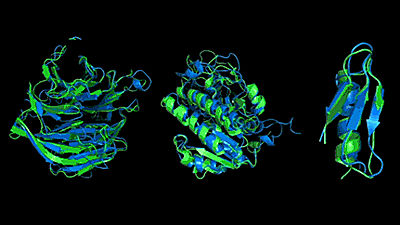
Googleの兄弟企業であり人工知能を研究するDeepMindが、遺伝子配列情報からタンパク質の立体構造を予測する技術「AlphaFold」を開発しました。正確なタンパク質の立体構造を理解することは、アルツハイマー病、パーキンソン病の新薬開発にも大きな発展をもたらすとみられています。
AlphaFold: Using AI for scientific discovery | DeepMind
https://deepmind.com/blog/alphafold/

タンパク質は筋肉を収縮させる、光を感知する、食物をエネルギーに変換するなど、人間の体が行うほぼ全ての機能に関連しています。タンパク質は20種類存在するL-アミノ酸が鎖状に多数連結した高分子化合物ですが、アミノ酸残基と呼ばれるアミノ酸の単位がどのようにつながっているのかは、一次元的な配列情報でしかDNAに記されていません。このため、タンパク質の三次元的な構造を予測することが「タンパク質の折りたたみ問題」と呼ばれる課題となっています。タンパク質が大きければ大きいほどモデル化は複雑かつ困難になるといわれています。
これまでの研究では低温電子顕微鏡法や核磁気共鳴、X線結晶学によってタンパク質の立体構造を明らかにしていましたが、いずれの方法も構造ごとに試行錯誤が必要で、非常にコストが高くつくものでした。そこで代わりとなる方法としてAIによる予測が注目されたわけですが、幸運にもここ数年で遺伝子解析技術が大きく進化したことで、遺伝子分野のデータを豊富に用意できたとのこと。そして、DeepMindはAlphaFoldを開発することに成功したわけです。
研究チームは過去に解決されたタンパク質折りたたみ問題を使用するのではなく、ターゲットとなる構造のモデリングにゼロから取り掛かりました。タンパク質構造が持つ物質的特性を予測した場合に、予測の正確性が高くなることが判明したため、研究チームは異なる2つの方法を用いて完全なタンパク質構造の予測を行ったとのことです。
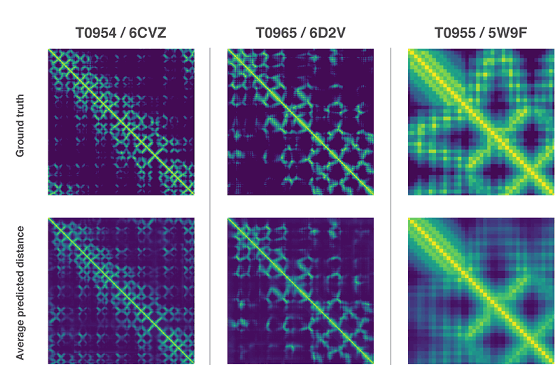
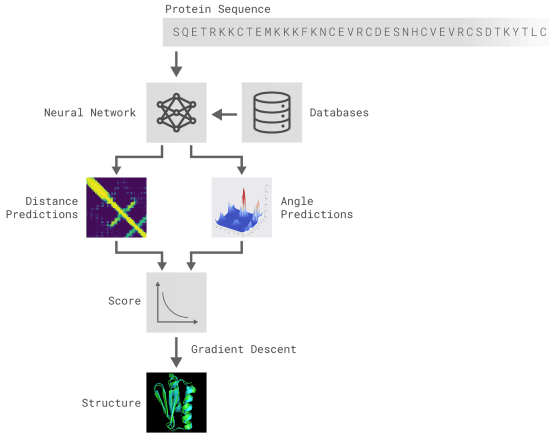
上記の2つの方法は、いずれも遺伝子配列からタンパク質の特性を予測するよう訓練されたニューラルネットワークを使うというもの。ネットワークが予測する特性は「アミノ酸のペアの距離」と「それらを結ぶ化学結合の間の角度」の2つです。この2つの予測から、どのくらい正確なタンパク質構造を提示できたのかがスコア化され、このスコアが機械学習を用いて最急降下法で最適化されたことにより、高い正確性で予測が可能になったとのこと。
アルツハイマー病、パーキンソン病、ハンチントン病、嚢胞性線維症といった病気の原因はタンパク質の間違った折りたたみが原因であると考えられており、タンパク質の構造を三次元的に予測し、理解を深めることは新しい薬の開発にも役立つと考えられています。また、タンパク質の折りたたみを理解することで生分解性酵素の分野での進歩があれば、プラスチックや油といった廃棄物の分解がより環境に配慮された形で行われるようになる可能性もあるとのことです。